开拓药业的新冠口服药终于迎来好消息。6日早上,开拓药业公布治疗新冠药物临床试验数据表现良好,随后开盘即爆发,其股价盘中一度暴涨超200%。截至发稿,公司股价报28.85港元,涨106.37%。
研发过程一波三折 曾因效果不佳股价跌去80%
今日,开拓药业在港交所公告,公布了普克鲁胺治疗轻中症非住院新冠患者III期临床试验(NCT04870606)的关键数据结果。
分析结果显示,普克鲁胺有效降低新冠患者(主要受Delta和Omicron变异株感染)的住院/死亡率,特别是对于服药超过7天的全部患者,以及伴有高风险因素的中高年龄新冠患者达到100%保护率,具有统计学显著性。同时,普克鲁胺可以显著降低新冠病毒载量,在症状改善方面,普克鲁胺组较对照组可更好地改善新冠肺炎的部分相关症状如发热、气短、咳嗽,且改善持续优于对照组到至少第28天。
在安全性数据方面,其临床试验结果显示,普克鲁胺治疗轻中症新冠受试者的整体耐受性良好,安全可控。整个 试验过程中,不良事件发生率分别为对照组7.9%及普克鲁胺组 9.6%,其中大部分为轻度,最常见的不良事件为眩晕(对照组及普克鲁胺组均为1.1%),其余任何一种不良事件发生率均﹤1%。研究中未发生任何严重不良事件。

图源:公司公告
开拓药业的新冠药物研发之路可谓一波三折。去年12月底,开拓药业公布了其在研新冠治疗药物“普克鲁胺”治疗轻中症非住院新冠患者III期临床试验的进展。结果显示,该项III期临床试验的中期分析未达到统计学显著性。开拓药业相关负责人当下向媒体强调,该试验没有失败,只是由于中期分析收集的事件数(住院人数)较少,遗憾没有达到统计学显著性。公司正在进行方案的调整,纳入高风险人群继续这项试验。对于这一次数据结果反转,开拓药业方面向媒体表示:“中期分析处于临床试验还未揭盲的状态,可以获知的数据很少,这次最终结果揭盲了,有更多的数据可以展现出来。”
疫苗科普专家陶黎纳表示,对于该试验结果还需要等到时间的考验,“要考虑数据的真实性以及试验设计是否会存在偏倚。”他认为三期临床试验如果效果真的显示良好,下一步可以申请上市。开拓药业创始人、董事长兼首席执行官童友之也在今日表示:“公司将积极推进向中国、美国及其他国家和地区的国家药物监督机构申请紧急用药EUA(应急使用授权)许可。”
新版诊疗方案纳入的新冠药物暂对无症状患者不适用
万联证券数据显示,目前国产新冠特效药有不少产品均取得了不错的进展,其中,君实生物的VV116、真实生物的阿兹夫定和开拓药业的普克鲁胺研发进展最快,均进入了3 期临床阶段。
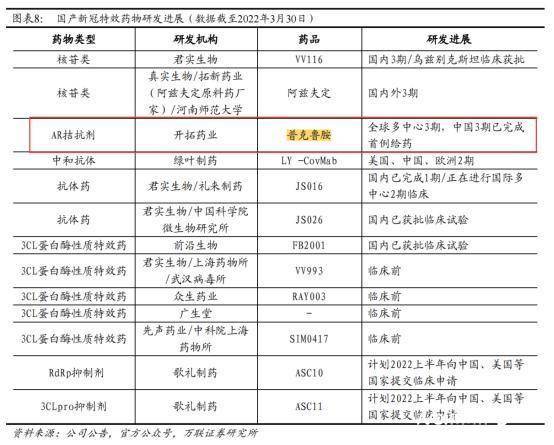
图源:万联证券
目前,君实药物的VV116已在乌兹别克斯坦获紧急使用授权。据了解,VV116正在开展全球多中心临床研究,其中3项在中国开展的I期研究已于近日完成,初步结果显示临床安全性良好,针对轻中度COVID-19患者的国际多中心II/III期临床试验正在进行中。年内通过临床试验后,将第一时间启动上市(NDA)申请。
在早前公开的新版诊疗方案中,新版诊疗方案将利托那韦片、安巴韦单抗/罗米司韦单抗注射液2款新冠抗病毒药物纳入抗病毒治疗中。
北京大学第一医院感染疾病科主任王贵强介绍,安巴韦单抗/罗米司韦单抗,这两个抗体是一个组合,都是针对新冠病毒的综合抗体。奈玛特韦片/利托那韦片则是小分子药物,属于合剂,是口服药物。
据了解,安巴韦单抗/罗米司韦单抗国内研发的、有独立自主知识产权的国产药物,小分子药物则是进口药。“这两个药,一个是通过中和病毒来发挥作用,就是中和抗体。第二个小分子药,通过抑制病毒的蛋白酶的水平,通过抑制蛋白酶阻断了病毒复制周期,减少了病毒复制,通过这个环节来抗病毒。这两个药有共同性,第一都有比较好的抗病毒作用,都可以有效降低住院和重症的风险。第二,适应症都是在轻型和普通型,具有重症高风险的人群来使用。”王贵强表示,目前这两类药物对于无症状感染者并不适用,主要是针对轻型和普通型,具有重症高风险的人群通过药物进行早期干预,阻断病情进展,降低重症和住院风险。“对目前的奥密克戎毒株,这两个药还是有效的。不同的地方是单克隆抗体需要静脉注射,静脉给药,而小分子药物是口服给药,当然这两个药使用的时间,静脉给药只用一次,口服给药是5天。当然我们强调,目前这两个药都在定点医院使用,在医生的指导之下严格按照说明书,要观察效果,同时要观察毒副作用,小分子药物之间的相互作用也要进行考虑。”





